Dalla ricerca alla pratica clinica
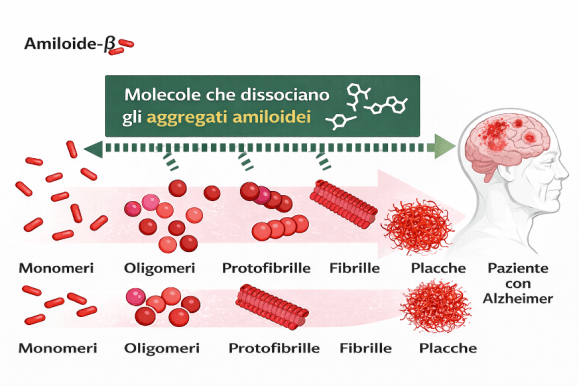
Nella malattia di Alzheimer il precoce accumulo di peptide beta-amiloide, insieme alla formazione e precipitazione della proteina tau iperfosforilata in grovigli neurofibrillari, rappresenta la firma patognomonica del processo neurodegenerativo e ne costituisce il nucleo biologico caratteristico. Pur non essendo l’unico determinante della cascata patogenetica, l’amiloide svolge certamente un ruolo essenziale nell’innescare e modulare questi eventi tau-correlati, che a loro volta si associano più direttamente alla progressione clinica della malattia.
Dalle prime vaccinazioni agli anticorpi monoclonali
Il primo tentativo clinico rilevante risale al vaccino AN1792 (immunizzazione attiva con peptide Aβ42). Un trial di fase I fu avviato nel dicembre 1999 (circa 80 pazienti). Successivamente, nell’ottobre 2001, partì uno studio di fase IIa, interrotto nel gennaio 2002 dopo la comparsa di meningoencefalite in 18 pazienti su 300 (6%). Nonostante l’interruzione, il follow-up fornì segnali biologici importanti (riduzione delle placche alla neuropatologia e, nei responder, possibile attenuazione del declino funzionale), ponendo le basi per approcci successivi più mirati e con maggiore controllo di dose e sicurezza.
Immunizzazione attiva e passiva: due strategie
In sintesi, gli approcci immunoterapici nell’Alzheimer possono essere distinti in:
Immunizzazione attiva: vaccini (es. AN1792, CAD106, ACI-24) che stimolano la produzione endogena di anticorpi anti-Aβ. AN1792 è stato sospeso per meningoencefalite; i candidati successivi hanno migliorato la sicurezza, ma con efficacia clinica finora limitata o variabile.
Immunizzazione passiva: somministrazione di anticorpi monoclonali (mAb) preformati, che consente titolazione della dose, maggiore prevedibilità e monitoraggio strutturato della sicurezza. È l’approccio che ha prodotto le evidenze cliniche più solide.
In parallelo, si è esteso l’interesse verso la proteina tau, la cui deposizione correla più strettamente con la gravità clinica. Immunoterapie anti-tau e strategie combinate rappresentano una frontiera in sviluppo.
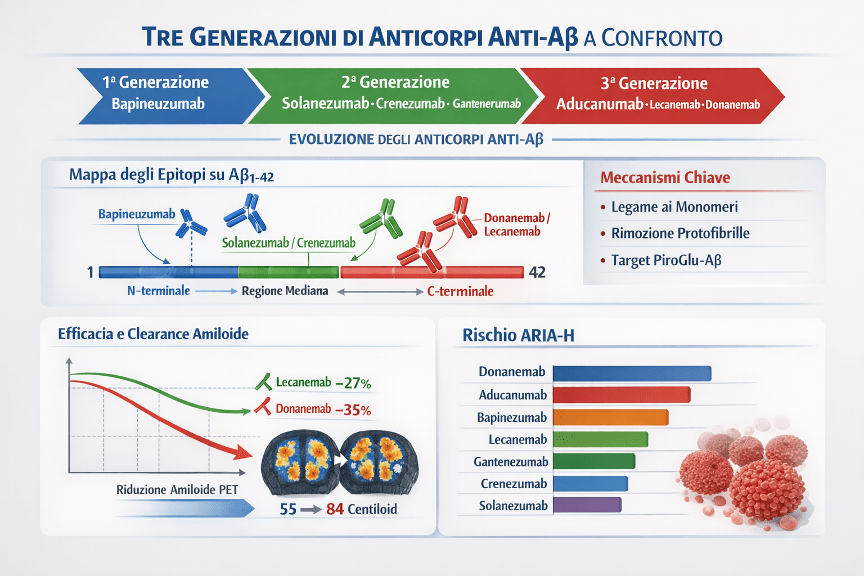
Tre generazioni di anticorpi anti-amiloide
Lo sviluppo dei mAb anti-Aβ può essere schematizzato in tre fasi:
Prima generazione: anticorpi diretti contro forme solubili o placche mature (es. solanezumab, bapineuzumab). Riduzioni amiloidi modeste o inconsistenti e assenza di beneficio clinico convincente.
Seconda generazione: maggiore affinità per aggregati e ottimizzazione della porzione Fc (es. gantenerumab, crenezumab). Migliore rimozione in alcuni studi, ma risultati clinici ancora limitati o negativi.
Terza generazione: maggiore selettività per specie aggregate/protofibrillari o epitopi specifici (es. lecanemab, donanemab). Clearance amiloide robusta e rallentamento clinico statisticamente significativo, con rischio ARIA che richiede monitoraggio.
Meccanismo d’azione (mAb di terza generazione)
I mAb anti-amiloide agiscono attraverso meccanismi in parte sovrapposti: opsonizzazione delle placche e fagocitosi microgliale mediata da recettori Fcγ; neutralizzazione di specie solubili tossiche (in particolare protofibrille per lecanemab); possibile facilitazione dell’efflusso e della degradazione di Aβ; e, in alcuni contesti, attivazione del complemento che contribuisce alla clearance. L’entità e la velocità della rimozione amiloide sono però anche correlate al rischio di ARIA.
Aducanumab: una lezione regolatoria
Aducanumab è stato approvato dalla FDA nel 2021 tramite percorso accelerato, ma con un rapporto beneficio-rischio ampiamente dibattuto e senza un chiaro consenso su un beneficio clinico significativo. L’EMA non lo ha approvato e lo sviluppo/commercializzazione sono stati poi interrotti. La vicenda ha rafforzato l’esigenza di standard rigorosi e trasparenza nella valutazione di farmaci modificanti la malattia.
Lecanemab (Leqembi): primo mAb anti-amiloide autorizzato nell’Unione Europea
Nello studio di fase III Clarity AD (18 mesi), lecanemab ha mostrato:
Riduzione del carico amiloide: nel braccio lecanemab -55,48 Centiloid vs +3,64 nel placebo; differenza trattamento-placebo -59,1 Centiloid (p<0,001).
Rallentamento del declino cognitivo-funzionale del 27% vs placebo su CDR-SB (differenza -0,45 punti; p<0,001).
Miglioramenti significativi anche su endpoint secondari (ADAS-Cog14, ADCOMS, ADCS-MCI-ADL).
I dati dell’estensione in aperto (OLE) fino a 36 mesi suggeriscono un mantenimento del beneficio, ma vanno interpretati con prudenza: il confronto è stato condotto rispetto a una coorte osservazionale esterna (ADNI) e non contro un braccio placebo randomizzato, con possibili bias di selezione e confondimento.
Delta CDR-SB di circa 0,95 punti rispetto al declino atteso nella coorte ADNI (con limiti metodologici intrinseci).
Riduzione del rischio relativo di progressione allo stadio successivo (HR 0,72; IC 95%: 0,59-0,87).
Segnali favorevoli su tau, neuroinfiammazione e biomarcatori di neurodegenerazione (pTau217, MTBR-tau243).
Profilo di sicurezza senza nuovi segnali, con ARIA prevalentemente nei primi 6 mesi.
Il percorso regolatorio europeo di Lecanemab è stato articolato: il 25 luglio 2024 il CHMP dell’EMA ha espresso parere negativo. Dopo richiesta di riesame e dati addizionali, il CHMP ha emesso parere positivo (novembre 2024). Nel gennaio 2025 la Commissione Europea ha richiesto un ulteriore riesame su dati di sicurezza; il 28 febbraio 2025 il CHMP ha riconfermato il parere positivo. L’autorizzazione all’immissione in commercio nell’UE è stata concessa il 15 aprile 2025.
In Italia, AIFA ha collocato Lecanemab in Classe C(nn) (farmaco non negoziato) in attesa della definizione di prezzo e rimborsabilità. Alcuni centri hanno avviato l’utilizzo in contesti controllati; ad esempio, l’IRCCS Ospedale San Raffaele di Milano ha iniziato la somministrazione da settembre 2024 nell’ambito di programmi gestiti in ambiente specialistico.
Donanemab (Kisunla): efficacia e trattamento a durata definita
Nello studio TRAILBLAZER-ALZ 2, donanemab ha mostrato un rallentamento clinico significativo, con effetti più pronunciati nella popolazione con tau basso/medio:Nella popolazione tau basso/medio: rallentamento del 35,1% su iADRS e del 36% su CDR-SB.Nella popolazione combinata (basso/medio + alto tau): rallentamento del 22,3% su iADRS e del 28,9% su CDR-SB.Nella popolazione tau basso/medio, circa l’80% ha raggiunto negatività amiloide alla PET, definita come <24,1 Centiloid (cutoff pre-specificato), consentendo l’interruzione della somministrazione.
Il percorso regolatorio europeo è stato complesso: dopo un primo parere negativo nel marzo 2025, il riesame ha portato a un parere positivo nel luglio 2025, principalmente attraverso una restrizione della popolazione eleggibile (esclusione degli omozigoti ApoE ε4) e misure di minimizzazione del rischio (programma di accesso controllato e RM seriali), non per una modifica del regime posologico. L’autorizzazione UE è stata concessa il 24 settembre 2025. Una peculiarità clinica è la durata definita del trattamento fino alla clearance amiloide. In Italia AIFA lo ha inserito, come gli altri nuovi anticorpi anti‑amiloide, in classe C(nn) subito dopo l’autorizzazione europea, con avvio del negoziato per prezzo e rimborsabilità secondo il nuovo regolamento HTA e le procedure descritte nel rapporto “Horizon Scanning 2025”, per cui la decisione su fascia di rimborso e condizioni prescrittive (probabile uso di registri AIFA e centri qualificati) è tuttora in corso.
Efficacia a confronto: cosa significa in pratica
Un confronto diretto tra lecanemab e donanemab richiede cautela per differenze tra popolazioni, criteri di inclusione (in particolare tau) ed endpoint. In pratica clinica, il bilancio beneficio-rischio dipende dallo stadio di malattia, dal profilo vascolare e dal genotipo ApoE ε4.
Beneficio clinico: statisticamente significativo ma di entità moderata; va discusso in termini di obiettivi realistici per paziente e caregiver.
Durata: donanemab può essere a durata definita (fino a negatività amiloide); lecanemab è concepito per trattamento continuativo.
Sicurezza: la rapidità di clearance sembra associarsi a un rischio maggiore di ARIA in Donanemab; la selezione del candidato, il monitoraggio RM e la gestione multidisciplinare sono centrali.
ARIA: l’evento avverso chiave
Le Amyloid-Related Imaging Abnormalities (ARIA) sono alterazioni rilevabili alla RM e rappresentano il principale limite di sicurezza dei mAb anti-amiloide:
ARIA-E: edema/effusione (edema vasogenico).
ARIA-H: microemorragie e siderosi superficiale.
I meccanismi proposti includono alterazione della barriera emato-encefalica, risposta infiammatoria e un quadro simile alla CAA-ri. Spesso gli ARIA sono asintomatici e si risolvono spontaneamente; quando sintomatici possono manifestarsi con cefalea, confusione, nausea o vertigini, e più raramente con convulsioni o encefalopatia.
Fattori che aumentano il rischio includono:
Genotipo ApoE ε4: rischio nettamente più alto negli omozigoti. In Clarity AD, le percentuali di ARIA-E sono state 32,6% negli omozigoti, 10,9% negli eterozigoti e 5,4% nei non-carrier; ARIA complessiva include anche ARIA-H.
Dose e fase iniziale del trattamento: maggiore incidenza nelle prime somministrazioni.
Velocità di clearance amiloide: rimozione più rapida correlata a rischio maggiore.
Un caso clinico emblematico ha descritto il decesso di un paziente ApoE ε4 omozigote trattato con lecanemab che, dopo un ictus, ha ricevuto trombolisi con t-PA e ha sviluppato multiple emorragie intracraniche; la neuropatologia ha evidenziato angiopatia amiloide cerebrale e vasculite. Il caso sottolinea la necessità di protocolli chiari per emergenze neurovascolari e di una valutazione rigorosa del rischio.
Eleggibilità e programma di accesso controllato (CAP)
Secondo l’indicazione autorizzata dall’EMA, il trattamento è destinato a:
Adulti con decadimento cognitivo lieve (MCI) o demenza lieve dovuti ad Alzheimer.
Conferma di patologia amiloide (PET o biomarcatori nel liquido cerebrospinale).
Pazienti ApoE ε4 non-carrier o eterozigoti (esclusi gli omozigoti).
RM cerebrale basale recente (entro 6 mesi), senza reperti suggestivi di elevato rischio emorragico/CAA.
Assenza di terapia anticoagulante in corso (secondo indicazioni e protocolli di sicurezza).
Il CAP richiede registrazione degli operatori e dei pazienti, materiale educazionale, e monitoraggio RM seriale. La somministrazione deve avvenire in ambiente idoneo, sotto supervisione di neurologi esperti e con accesso tempestivo alla neuroradiologia.
Scenario italiano: sfide organizzative
In Italia si stimano circa 1,2 milioni di persone con demenza, di cui circa 700.000 con Alzheimer e circa 950.000 con deterioramento cognitivo lieve. Nel contesto UE/Italia, la negoziazione di prezzo e rimborsabilità è in corso; i listini USA (circa 26.500 dollari/anno per lecanemab e 32.000 dollari/anno per donanemab) non sono direttamente trasferibili al contesto europeo e vanno intesi come riferimento statunitense. Una parte rilevante del costo deriva inoltre dal monitoraggio RM e dall’organizzazione di percorsi dedicati.
Per garantire equità di accesso servono: potenziamento della diagnosi precoce, disponibilità omogenea di biomarcatori (inclusi quelli plasmatici, quando validati), e formazione dei professionisti alla gestione di terapie complesse con protocolli di sicurezza condivisi.
Prospettive
Le immunoterapie anti-amiloide rappresentano un avanzamento significativo ma non risolutivo. Le principali direttrici future includono:
Terapie combinate (anti-amiloide + anti-tau e/o anti-neuroinfiammazione).
Target alternativi e interventi a monte del processo neurodegenerativo.
Riduzione degli eventi avversi tramite selezione basata su rischio vascolare e genetico e ottimizzazione dei protocolli RM.
Ottimizzazione dei tempi: strategie a durata definita (come con donanemab) e schemi più sostenibili.
Medicina di precisione basata su profilo genetico, carico di tau e stadio clinico.
Conclusioni
L’autorizzazione nell’Unione Europea di lecanemab (15 aprile 2025) e donanemab (24 settembre 2025) segna un cambio di paradigma: per la prima volta sono disponibili terapie che incidono sul processo patogenetico e non solo sui sintomi. Il beneficio clinico è in media moderato e richiede comunicazione trasparente, selezione rigorosa dei candidati e monitoraggio strutturato del rischio ARIA. Il valore reale di queste terapie dipenderà dalla capacità di integrarle in percorsi organizzati, equi e sostenibili, con un approccio di medicina di precisione.
—
Articolo basato sulla presentazione del 11 gennaio 2025 presso l’Ospedale Niguarda di Milano (“Immunoterapie per la malattia di Alzheimer”) del Dr. Luigi Giovanni Manfredi, con aggiornamenti allo stato dell’arte a febbraio 2026.
Fonti
[1] Malattia di Alzheimer, le ultime novità su donanemab e… https://neuroinfo.it/speciale/neurodegenerative/malattia-di-alzheimer-le-ultime-novita-su-donanemab-e-lecanemab/
[2] The Lecanemab Clarity AD Open-Label Extension in Early Alzheimer’s Disease (P1-3.003) | Neurology https://www.neurology.org/doi/10.1212/WNL.0000000000211489
[3] Lecanemab nei pazienti con Alzheimer lieve, benefici… https://www.doctor33.it/articolo/64118/lecanemab-nei-pazienti-con-alzheimer-lieve-benefici-sostenuti-per-36-mesi
[4] Lecanemab approved in Europe for the treatment of early-… https://www.gsdinternational.com/news/alzheimer-s-lecanemab-approved-in-europe-for-the-treatment-of-early-stage-disease
[5] EU Commission approves Leqembi for treatment of Alzheimer https://www.eanpages.org/2025/04/17/eu-commission-approves-leqembi-lecanemab-for-treatment-of-early-stage-alzheimers-disease/
[6] Alzheimer: approvato in Europa il primo farmaco per le fasi iniziali https://www.doctor33.it/articolo/64160/alzheimer-approvato-in-europa-il-primo-farmaco-per-le-fasi-iniziali
[7] Gazzetta n. 165 del 18 luglio 2025 – AGENZIA ITALIANA DEL… http://www.gazzettaufficiale.biz/atti/2025/20250165/25A04004.htm
[8] EMA approves marketing authorization for donanemab for… – BBRC https://www.barcelonabeta.org/en/news/news/ema-approves-marketing-authorization-donanemab-early-stage-alzheimers-treatment
[9] European commission grants a marketing authorisation for anti… https://www.alzheimer-europe.org/news/european-commission-grants-marketing-authorisation-anti-amyloid-drug-donanemab?language_content_entity=en
[10] The EMA issues a negative opinion on the authorization of… https://www.barcelonabeta.org/en/news/news/ema-issues-negative-opinion-authorization-donanemab-treatment-alzheimers-disease
[11] Alzheimer: la strategia dell’Agenzia italiana del farmaco… https://www.aboutpharma.com/sanita-e-politica/alzheimer-la-strategia-dellagenzia-italiana-del-farmaco-per-gestire-le-nuove-terapie-in-arrivo/
[12] ecco l’onda dei nuovi medicinali approvati dall’EMA https://www.aifa.gov.it/-/l-onda-dei-nuovi-medicinali-approvati-da-ema
[13] Alzheimer: ricerca, prospettive e strategie di cura https://www.aifa.gov.it/-/alzheimer-ricerca-prospettive-e-strategie-di-cura
[14] Alzheimer, ok dell’Ema all’autorizzazione di donanemab in fase… https://www.farmacista33.it/farmaci/31629/alzheimer-ok-dell-ema-all-autorizzazione-di-donanemab-in-fase-precoce.html
[15] “Rischi gravi e costi alti degli anticorpi monoclonali… https://www.alzheimer-riese.it/contributi-dal-mondo/ricerche/11941-rischi-gravi-e-costi-alti-degli-anticorpi-monoclonali-possono-superare-i-benefici-nell-alzheimer